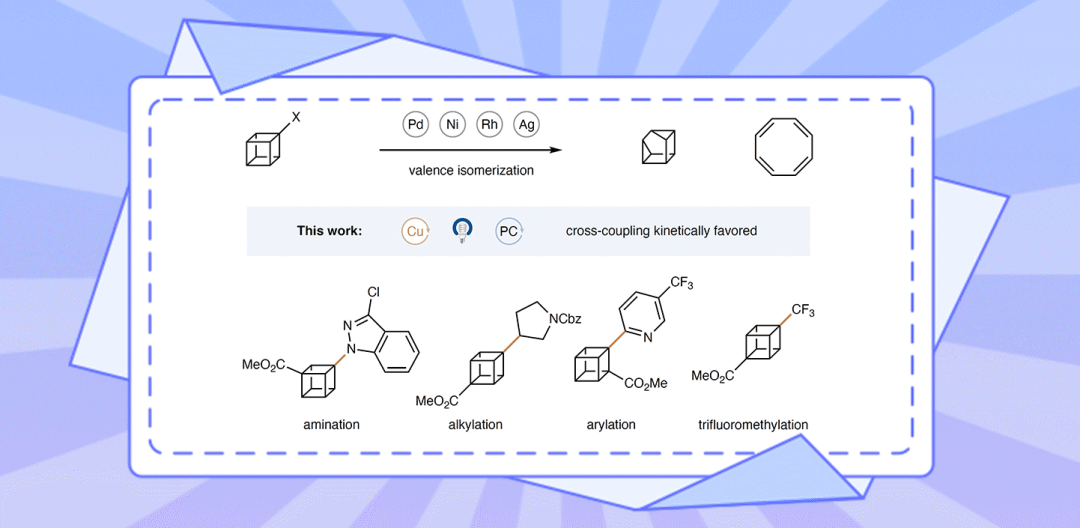
 在众多的候选药物中,利用sp3杂化的生物电子等排体来替代苯可以在保留其生物活性的同时有效改善药物的药代动力学性质。具有较高环张力的刚性分子骨架双环[1.1.1]戊烷和立方烷由于具有较高的C-H键能,其代谢稳定性得到有效提高,因此可以作为苯环的生物电子等排体。特别是立方烷,由于其与苯的几何构型最为匹配,因此可以作为一类理想的苯环生物电子等排体来使用。然而,在目前药物设计过程中,立方烷大多仅作为单取代苯或对二取代苯的替代结构。而其它取代类型的立方烷,如1,3-和1,2-二取代立方烷,由于难以合成且在过渡金属催化的偶联反应中兼容性差,因此较少应用于药物设计中。最近,2021年诺贝尔化学奖得主、美国普林斯顿大学默克催化中心(Merck Center for Catalysis at Princeton University)的David W. C. MacMillan教授率领研究团队首次使用简单易得的环丁二烯作为前体,通过光解C-H羧基化反应分别实现了1,3-和1,2-二取代立方烷的制备。此外,作者基于铜缓慢的氧化加成和快速还原消除的特性,发展了光/铜共催化二取代立方烷的C-N, C-C(sp3), C-C(sp2)和C-CF3偶联反应。相关成果发表在Nature上(DOI: 10.1038/s41586-023-06021-8)(Fig. 1)。
在众多的候选药物中,利用sp3杂化的生物电子等排体来替代苯可以在保留其生物活性的同时有效改善药物的药代动力学性质。具有较高环张力的刚性分子骨架双环[1.1.1]戊烷和立方烷由于具有较高的C-H键能,其代谢稳定性得到有效提高,因此可以作为苯环的生物电子等排体。特别是立方烷,由于其与苯的几何构型最为匹配,因此可以作为一类理想的苯环生物电子等排体来使用。然而,在目前药物设计过程中,立方烷大多仅作为单取代苯或对二取代苯的替代结构。而其它取代类型的立方烷,如1,3-和1,2-二取代立方烷,由于难以合成且在过渡金属催化的偶联反应中兼容性差,因此较少应用于药物设计中。最近,2021年诺贝尔化学奖得主、美国普林斯顿大学默克催化中心(Merck Center for Catalysis at Princeton University)的David W. C. MacMillan教授率领研究团队首次使用简单易得的环丁二烯作为前体,通过光解C-H羧基化反应分别实现了1,3-和1,2-二取代立方烷的制备。此外,作者基于铜缓慢的氧化加成和快速还原消除的特性,发展了光/铜共催化二取代立方烷的C-N, C-C(sp3), C-C(sp2)和C-CF3偶联反应。相关成果发表在Nature上(DOI: 10.1038/s41586-023-06021-8)(Fig. 1)。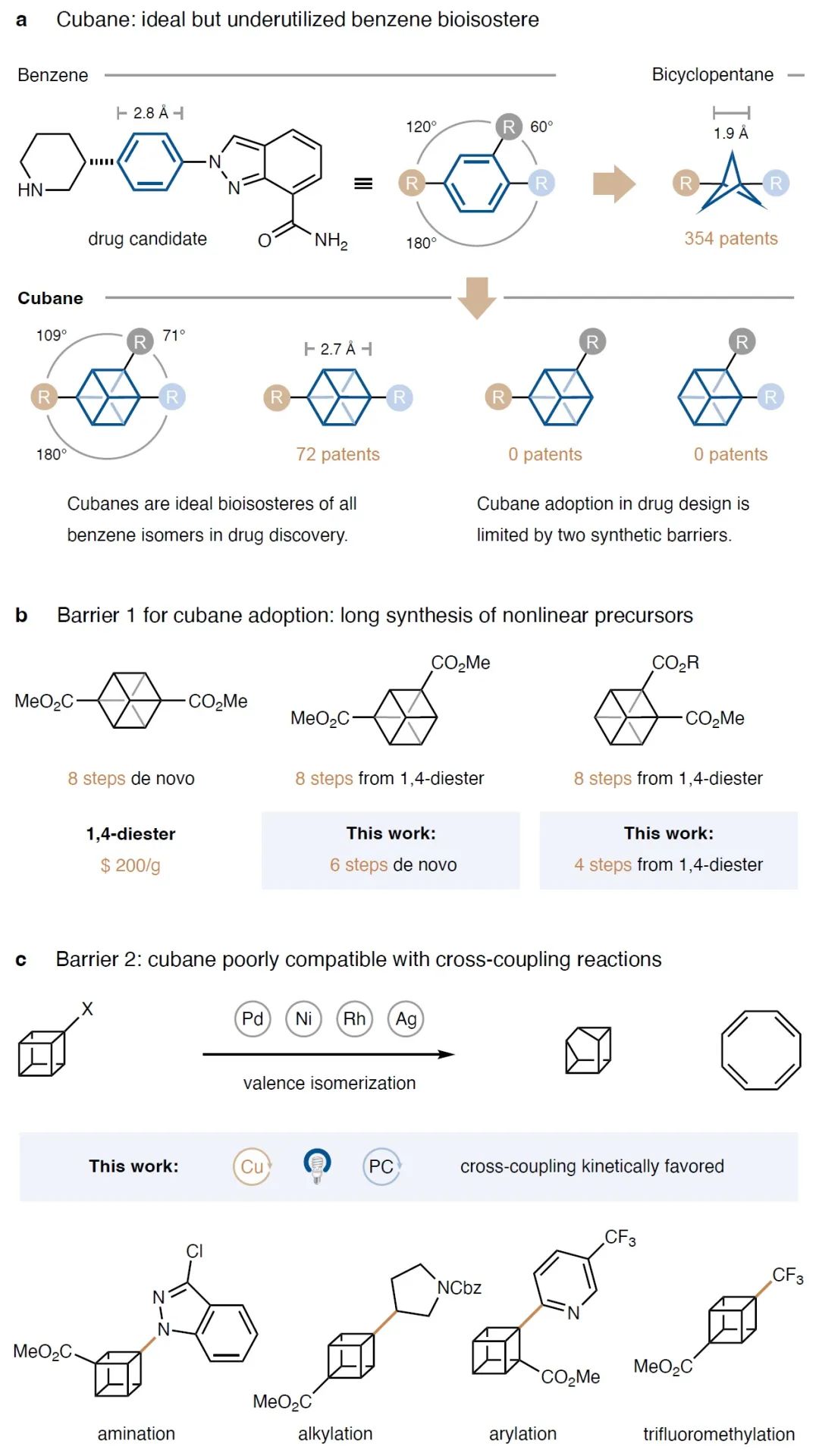
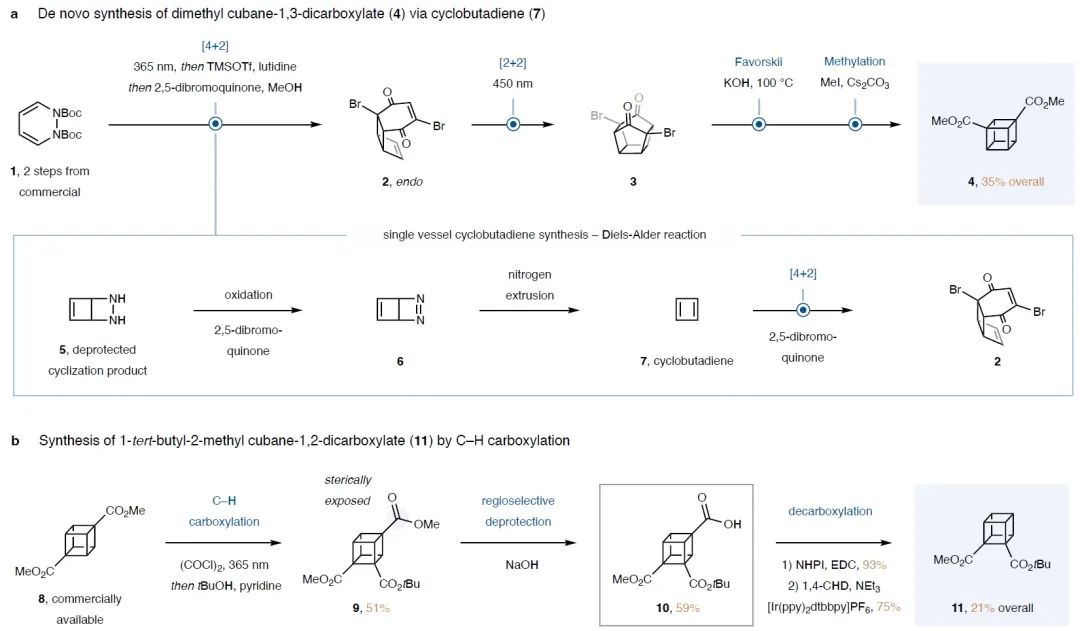
 虽然1966年Pettit 基于Diels-Alder反应的3步合成转化实现了立方烷-1,3-二羧酸的合成(J. Am. Chem. Soc. 1966, 88, 1328)。但是由于反应底物不易得且反应过程中需要使用多种剧毒化学品,使得此转化并未广泛应用于药物研发中。因此,发展简洁高效的合成方法,在温和的反应条件下实现1,3-立方烷的合成具有重要意义。基于Masamune小组的研究工作(J. Am. Chem. Soc. 1975, 97, 918),作者选用1,2-二氢哒嗪1作为起始原料,通过[4+2]环加成、分子内[2+2]环加成、Favorskii缩环、甲基化四步以35%的产率实现了立方烷-1,3-二羧酸酯4的合成。值得注意的是,此合成方法仅需要经历一次柱层析过程,可以在3天内即可实现立方烷-1,3-二羧酸酯的合成。然而,此方法并不适用于相应的立方烷-1,2-二羧酸酯的合成。作者认为可能是由于其会发生Haller-Bauer断裂所导致的,而利用C-H官能团化反应则可以避免此问题。随后,作者利用商业可得的立方烷-1,4-二羧酸甲酯8作为起始原料,通过C-H羧基化、酯化、区域选择性脱保护以及脱羧4步,以21%的总产率实现了立方烷-1,2-二羧酸酯11的合成(Fig. 2)。在实现了立方烷二羧酸酯的合成后,作者对立方烷二羧酸酯参与的偶联反应进行了探索(Fig. 3)。基于文献报道,实现此类转化的关键在于立方烷骨架与过渡金属催化剂要兼容。因此,作者选择使用廉价易得的铜最为金属催化剂,利用其缓慢氧化加成和快速还原消除的特性,可以有效抑制立方烷骨架的分解。接下来,作者发展了光/铜共催化的反应策略,利用商业可得的1,4-二取代的立方烷作为起始原料,实现了C(sp3)-N键的构建,以51-85%的产率合成了一系列胺化立方烷18-29,此类化合物可以作为苯胺的生物电子等排体应用于药物研发过程中。值得注意的是,此方法是继Curtius重排之后另一个胺化立方烷的通用合成策略。除此之外,作者还发展了光/铜共催化策略,通过立方烷自由基与烷基或芳基自由基偶联,实现了C-C键的构建。实验结果表明不同取代的溴化物均可以与立方烷发生偶联,以41-52%的产率得到产物33-46。值得注意的是,作者使用Umemoto试剂作为三氟甲基源,成功实现了C(sp3)-CF3键的构建,以49%的产率得到三氟甲基化产物47。
虽然1966年Pettit 基于Diels-Alder反应的3步合成转化实现了立方烷-1,3-二羧酸的合成(J. Am. Chem. Soc. 1966, 88, 1328)。但是由于反应底物不易得且反应过程中需要使用多种剧毒化学品,使得此转化并未广泛应用于药物研发中。因此,发展简洁高效的合成方法,在温和的反应条件下实现1,3-立方烷的合成具有重要意义。基于Masamune小组的研究工作(J. Am. Chem. Soc. 1975, 97, 918),作者选用1,2-二氢哒嗪1作为起始原料,通过[4+2]环加成、分子内[2+2]环加成、Favorskii缩环、甲基化四步以35%的产率实现了立方烷-1,3-二羧酸酯4的合成。值得注意的是,此合成方法仅需要经历一次柱层析过程,可以在3天内即可实现立方烷-1,3-二羧酸酯的合成。然而,此方法并不适用于相应的立方烷-1,2-二羧酸酯的合成。作者认为可能是由于其会发生Haller-Bauer断裂所导致的,而利用C-H官能团化反应则可以避免此问题。随后,作者利用商业可得的立方烷-1,4-二羧酸甲酯8作为起始原料,通过C-H羧基化、酯化、区域选择性脱保护以及脱羧4步,以21%的总产率实现了立方烷-1,2-二羧酸酯11的合成(Fig. 2)。在实现了立方烷二羧酸酯的合成后,作者对立方烷二羧酸酯参与的偶联反应进行了探索(Fig. 3)。基于文献报道,实现此类转化的关键在于立方烷骨架与过渡金属催化剂要兼容。因此,作者选择使用廉价易得的铜最为金属催化剂,利用其缓慢氧化加成和快速还原消除的特性,可以有效抑制立方烷骨架的分解。接下来,作者发展了光/铜共催化的反应策略,利用商业可得的1,4-二取代的立方烷作为起始原料,实现了C(sp3)-N键的构建,以51-85%的产率合成了一系列胺化立方烷18-29,此类化合物可以作为苯胺的生物电子等排体应用于药物研发过程中。值得注意的是,此方法是继Curtius重排之后另一个胺化立方烷的通用合成策略。除此之外,作者还发展了光/铜共催化策略,通过立方烷自由基与烷基或芳基自由基偶联,实现了C-C键的构建。实验结果表明不同取代的溴化物均可以与立方烷发生偶联,以41-52%的产率得到产物33-46。值得注意的是,作者使用Umemoto试剂作为三氟甲基源,成功实现了C(sp3)-CF3键的构建,以49%的产率得到三氟甲基化产物47。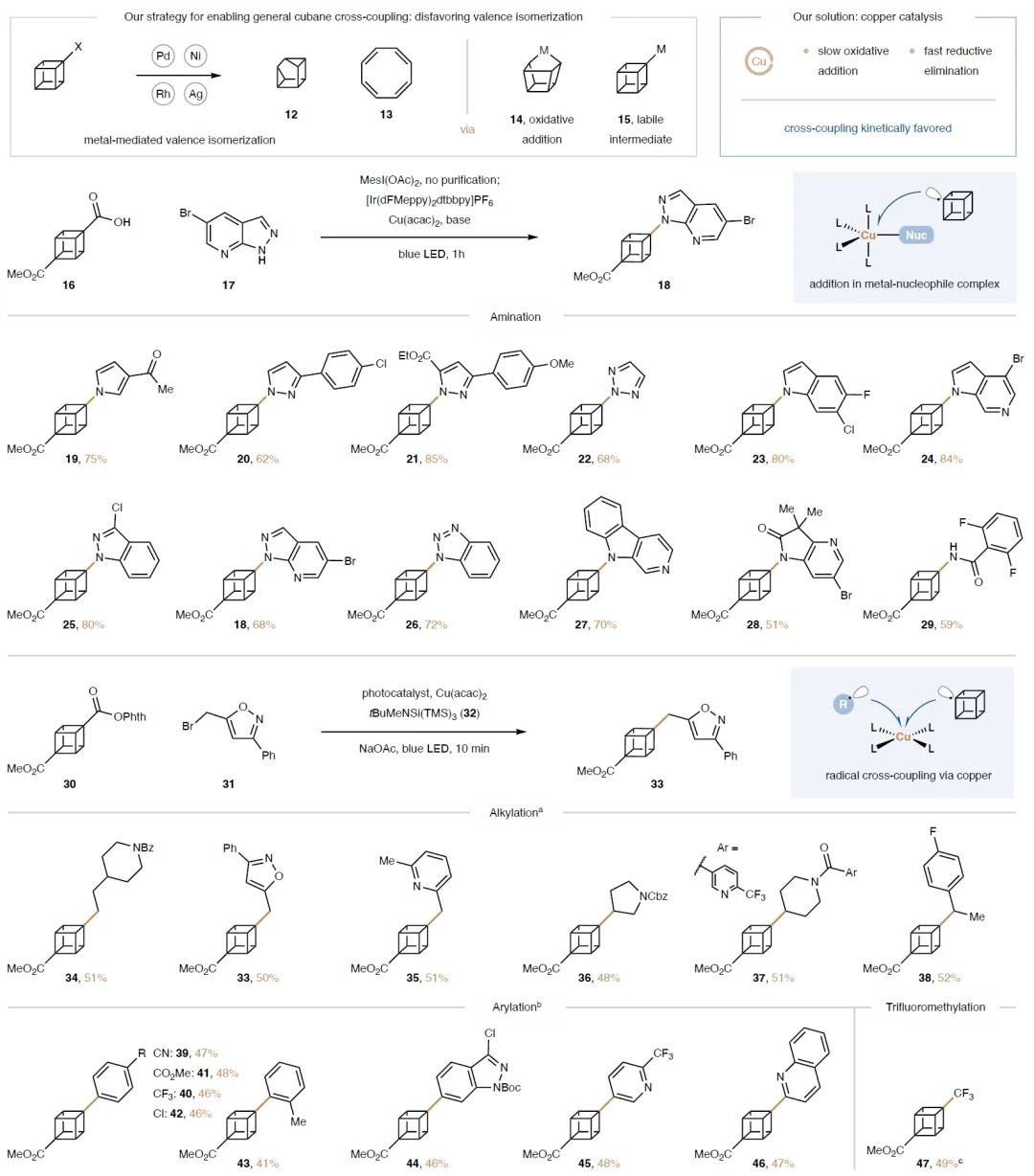
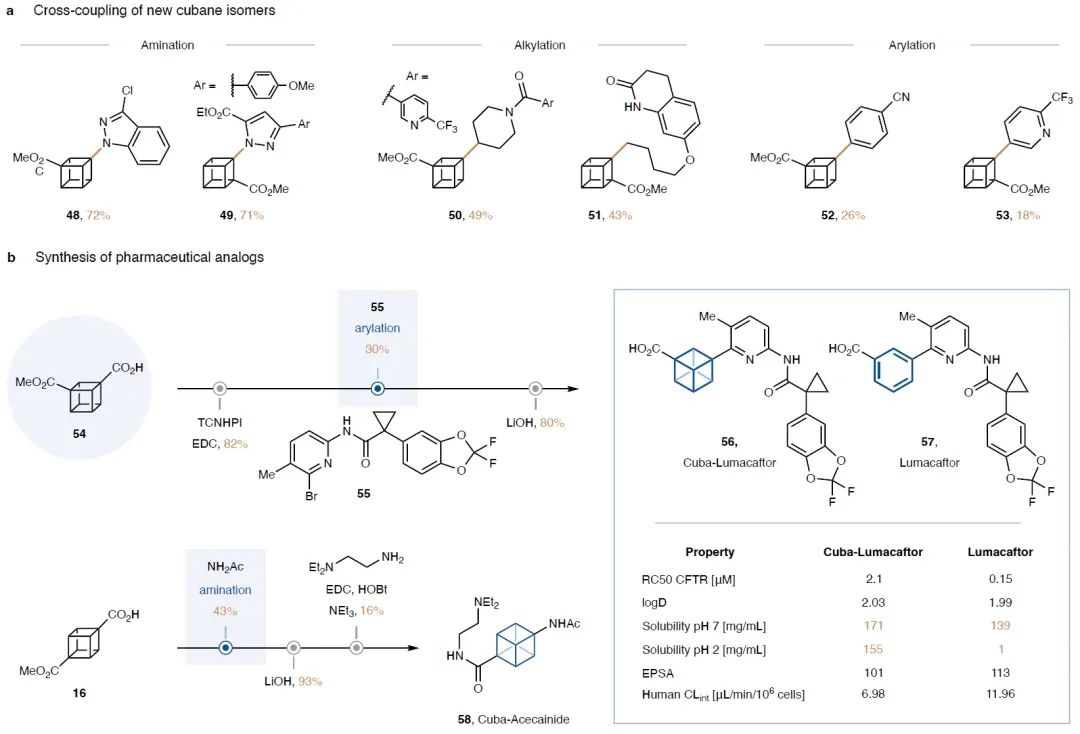
最后,作者利用发展出的方法探索了1,3-和1,2-二取代立方烷的偶联(Fig. 4a)。实验结果表明1,3-和1,2-二取代立方烷也可以顺利实现胺化和烷基化过程,但是芳基化过程产率相对较低。此外,作者利用此方法还成功实现了药物分子Cuba-Lumacaftor和Cuba-Acecainide的合成。随后作者通过生物活性测试得出Cuba-Lumacaftor与Lumacaftor相比具有更高的生物活性,并且Cuba-Acecainide与Acecainide相比在溶解性上有所提高(Fig. 4b)。
David W. C. MacMillan教授研究团队首次使用简单易得的环丁二烯作为前体,通过光解C-H羧基化反应分别实现了1,3-和1,2-二取代立方烷的实验室规模制备。此外,作者鉴于铜缓慢的氧化加成和快速还原消除的特性,发展了光/铜共催化二取代立方烷的C-N, C-C(sp3), C-C(sp2)和C-CF3偶联反应。此反应策略为苯的立方烷类生物电子等排体骨架的合成提供了新的思路。General Access to Cubanes as Benzene BioisosteresMario P. Wiesenfeldt, James A. Rossi-Ashton, Ian B. Perry, Johannes Diesel, Olivia L. Garry, Florian Bartels, Susannah C. Coote, Xiaoshen Ma, Charles S. Yeung, David J. Bennett& DavidW. C. MacMillanNature DOI: 10.1038/s41586-023-06021-8 本文授权转载自微信公众号「CBG资讯」,未经许可谢绝二次转载,如需转载请联系C菌(微信号:chembeango101)