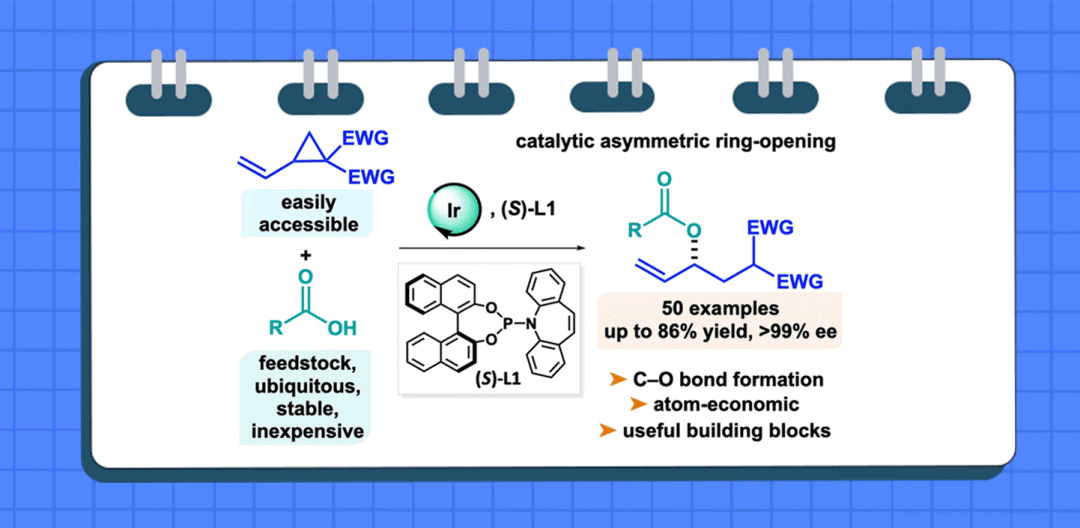
近日,印度科学与创新研究院(AcSIR)Nilanjana Majumdar课题组开发了一种铱催化非活化羧酸(作为氧亲核试剂)与乙烯基环丙烷的高度区域与对映选择性烯丙基取代反应,合成了一系列具有价值的手性砌块,具有高收率、高原子经济性等特点。作者通过后期衍生化实验,进一步证明了反应的实用性。相关研究成果发表在ACS Catal.上(DOI: 10.1021/acscatal.3c00959)。


供体-受体环丙烷可与多种亲偶极体(dipolarophiles)进行环化反应。其中,由于双键的存在,乙烯基环丙烷(VCPs)(1)是一种特殊类型的供体-受体环丙烷。在过渡金属催化剂存在下,VCPs(1)经开环后可生成偶极配合物(2),并可进行各种环加成反应(Chart 1A)。因此,化学家们已开发多种过渡金属催化乙烯基环丙烷的不对称环加成反应。相比之下,亲核试剂或亲电试剂与乙烯基环丙烷的催化不对称开环反应却较少有相关的研究。目前为止,仅有少数涉及C-亲核试剂的开环反应,但对于O-亲核试剂与VCPs的不对称开环反应,仍有待进一步的研究。近日,印度科学与创新研究院(AcSIR)Nilanjana Majumdar课题组开发了一种手性铱催化非活化羧酸(作为氧亲核试剂)与乙烯基环丙烷的对映选择性烯丙基取代反应,合成了一系列手性烯丙基酯衍生物(Chart 1B)。
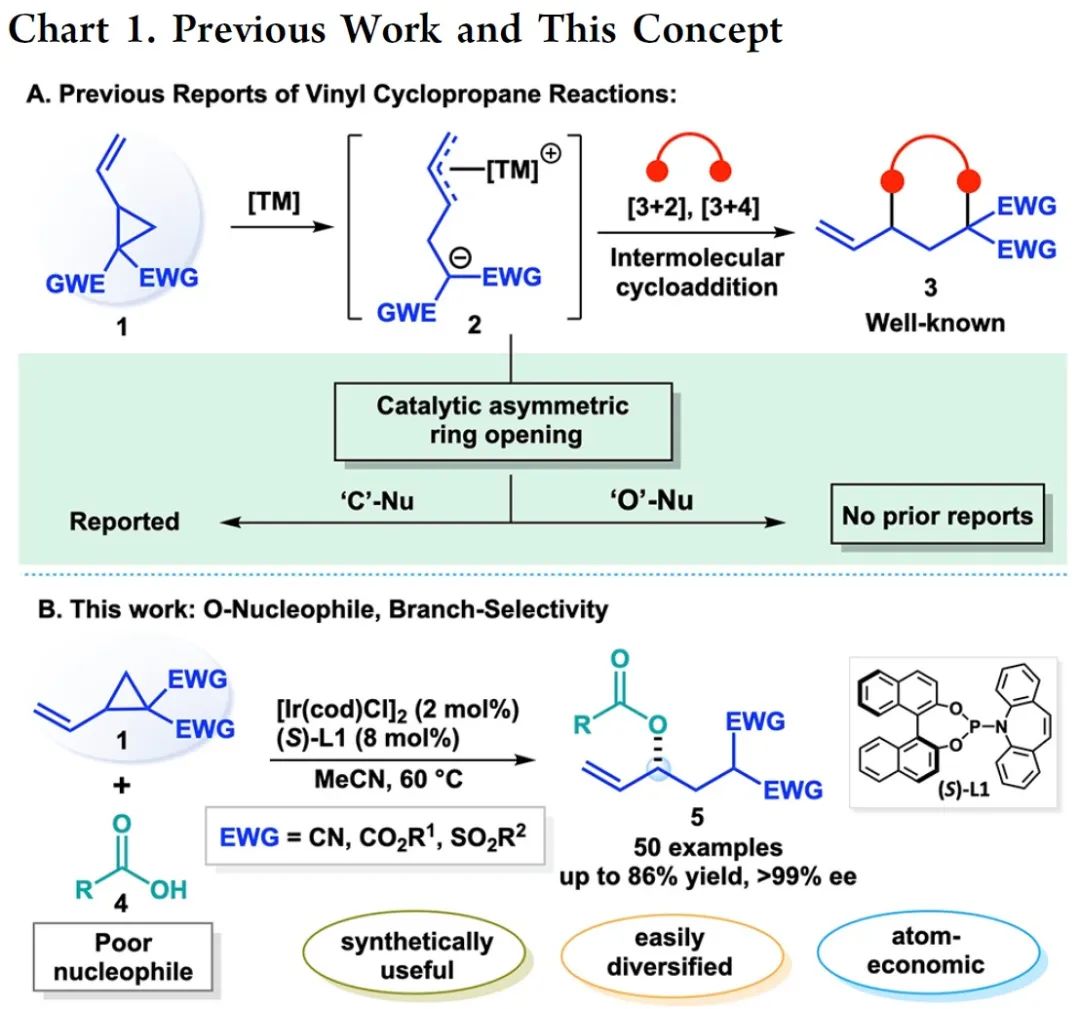
(图片来源:ACS Catal.)
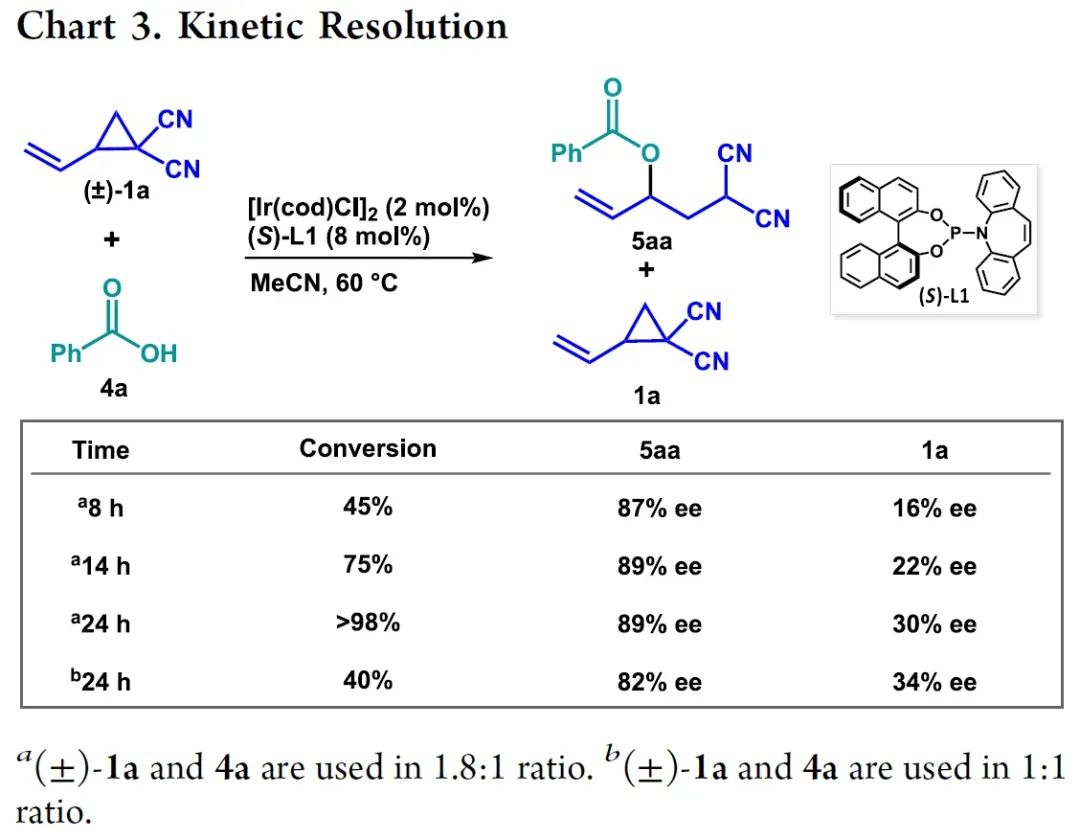
首先,作者以乙烯基环丙烷衍生物(±)-1a与苯甲酸4a作为模型底物,对反应条件进行了大量的筛选(Table 1)。筛选结果表明,当以[Ir(cod)Cl]2作为催化剂,(S)-L1作为手性配体,乙腈作为溶剂,在60℃下反应,可以以>90%的转化率的得到产物5aa,ee为90%。
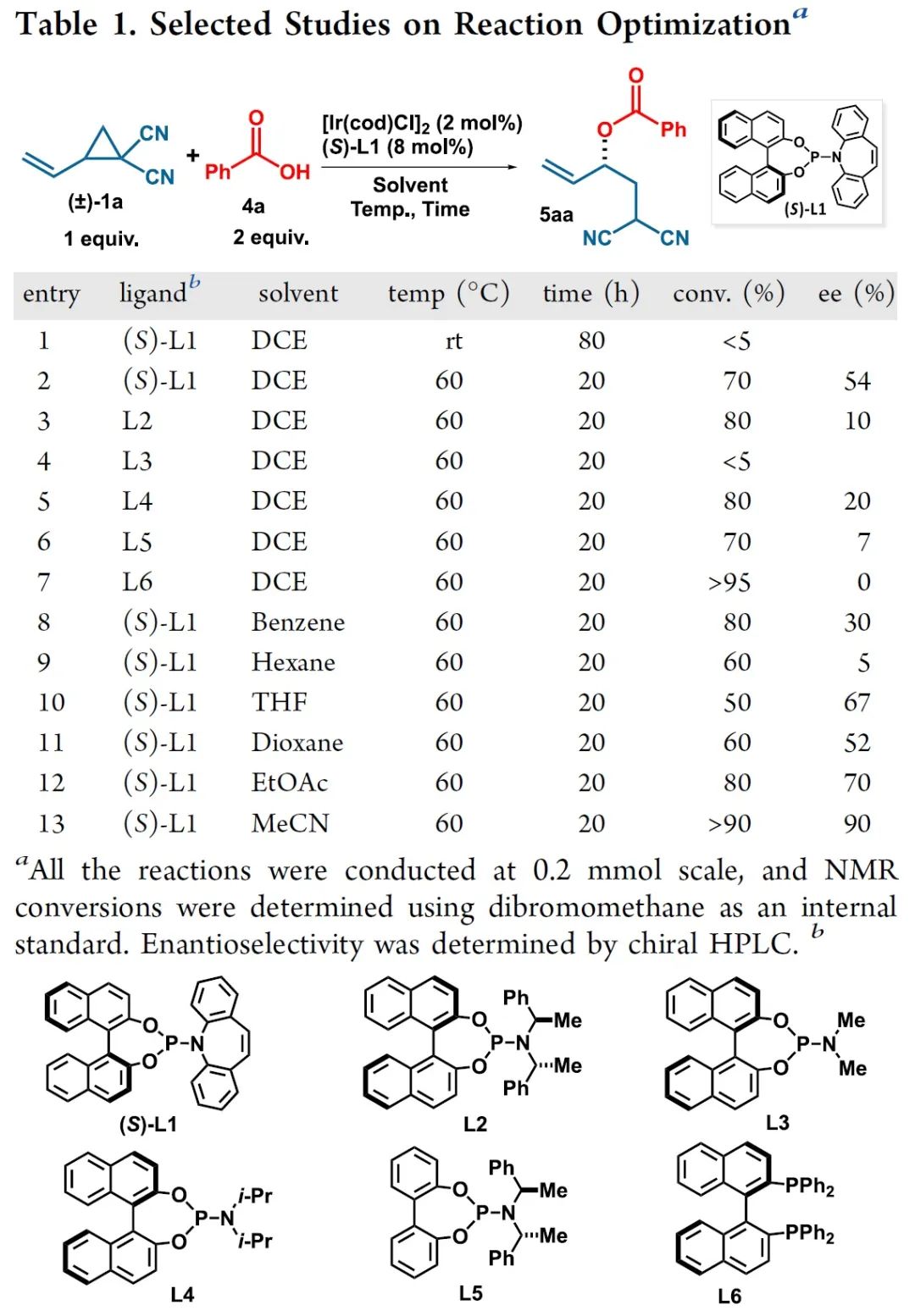
(图片来源:ACS Catal.)
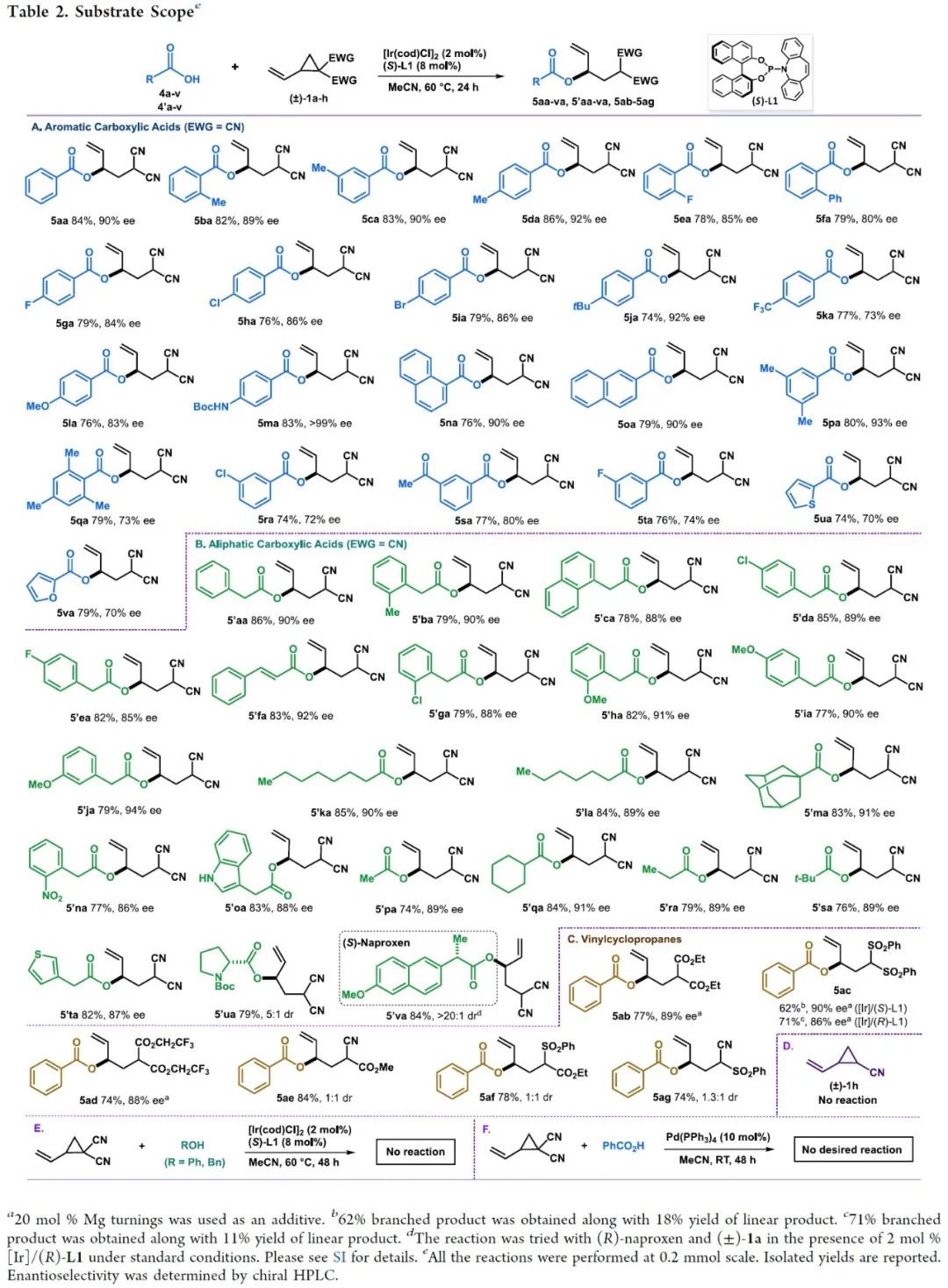
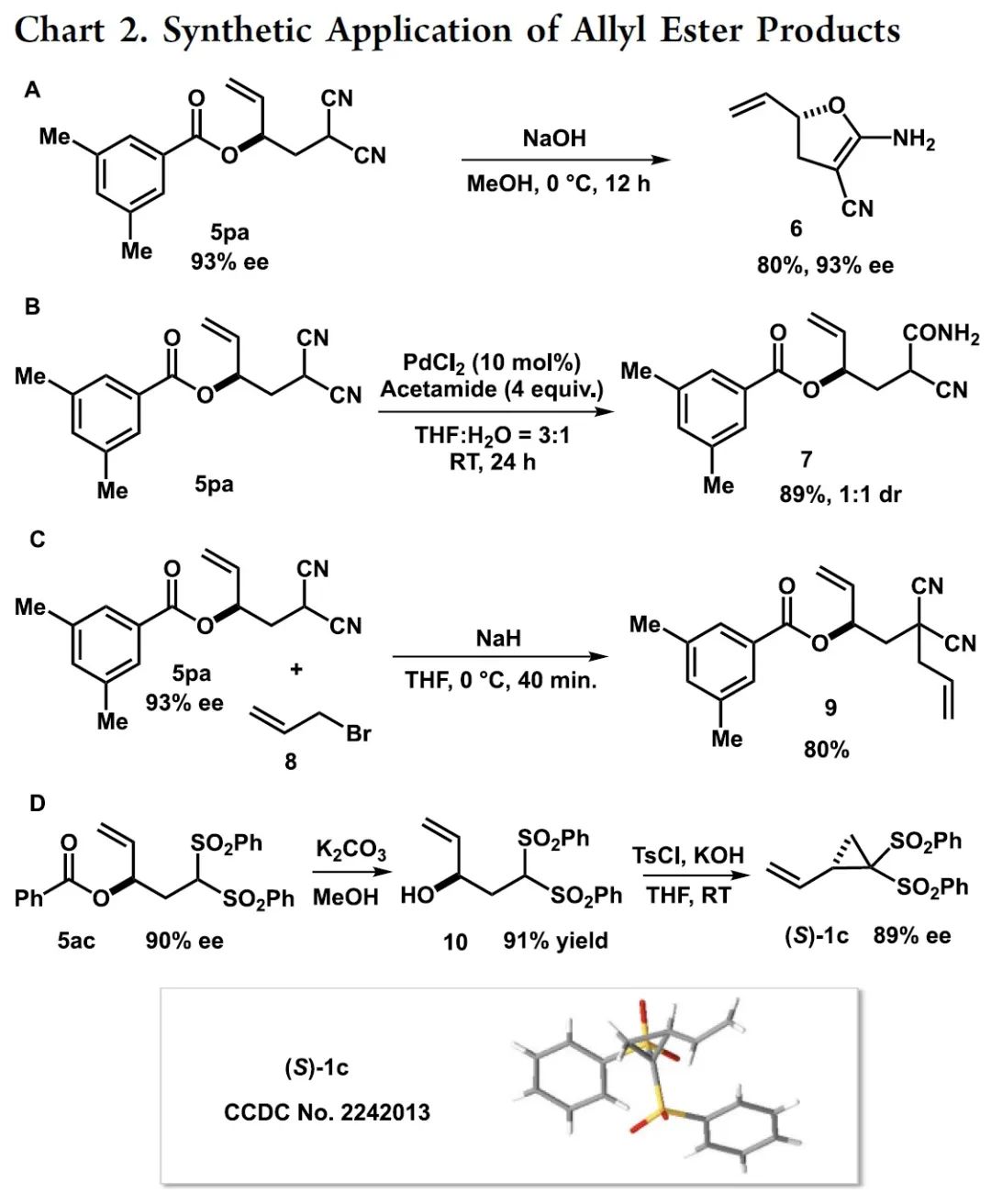
在获得上述最佳反应条件后,作者对底物范围进行了扩展(Table 2)。首先,一系列不同电性取代的苯甲酸底物均可顺利进行反应,获得相应的产物5aa-5ma和5pa-5ta,收率为76-86%,ee为73->99%(Table 2A)。值得注意的是,与含有吸电子取代基的底物相比,含有供电子取代基的底物具有更高的对映选择性。同时,1-/2-萘甲酸、噻吩-2-羧酸和2-糠酸均为合适的底物,获得相应的产物5na、5oa、5ua和5va,收率为74-79%,ee为70-90%。其次,一系列不同取代的脂肪族羧酸,也能够顺利进行反应,获得相应的产物5′aa-5′va,收率为76-86%,ee为85-94%(Table 2B)。其中,Boc-保护的D-脯氨酸(5′ua)和(S)-萘普生(5′va),均与体系兼容。此外,通过对反应条件的再次优化后发现,一系列含有各种不同吸电子基团的VCPs,均可与苯甲酸顺利反应,获得相应的产物5ab-5ag,收率为62-84%(Table 2C)。然而,含有单氰基取代的VCP底物(±)-1h未能顺利进行反应(Table 2D)。同时,(±)-1a与更具反应性的脂肪族和芳香族醇底物(如苯酚和苯甲醇)反应时,也未能进行相应的反应(Table 2E)。(±)-1a与苯甲酸在(PPh3)4催化下反应时,也未能获得所需的目标产物(Table 2F)。


本文授权转载自微信公众号「CBG资讯」,未经许可谢绝二次转载,如需转载请联系C菌(微信号:chembeango101)