近日,Cimeio Therapeutics宣布,将与宾夕法尼亚大学Perelman医学院细胞免疫疗法中心的Saar Gill博士开展临床前合作,以研究和评估一种靶向CD45的通用CAR-T细胞的血液肿瘤治疗潜力。
CD45是较少见的药物开发靶点,主要原因是其在除红细胞和血小板外的所有造血干细胞(HSCs)中均有表达。因此,尽管CD45具有控制免疫系统信号通路的作用,以及在血液肿瘤细胞中高表达,具有作为药物靶标开发潜力,但还是鲜有人去开发CD45。
如果按照传统的CAR-T细胞治疗去设计和开发CD45 CAR-T细胞,是不行的。
因为会导致CD45 CAR-T无差别攻击表达CD45的细胞,无论是肿瘤细胞还是正常细胞,会造成严重的毒副作用。
但也有一个好处就是,CD45 CAR-T可以攻击所有表达CD45的细胞,即可以用于所有的血液肿瘤,成为一种血液肿瘤通用的CAR-T细胞治疗,因为几乎所有血细胞上都高度表达CD45。
延伸阅读:CD45: 不再只是一个marker
为了实现CD45 CAR-T的肿瘤杀伤作用,同时保证安全性,Cimeio公司和宾大团队进行合作,结合Cimeio公司专有的Shielded Cell & Immunotherapy Pairs™(细胞屏蔽技术和配对免疫技术),开发CD45 CAR-T细胞与配对的CD45表位编辑造血干细胞(HSC)组合疗法。
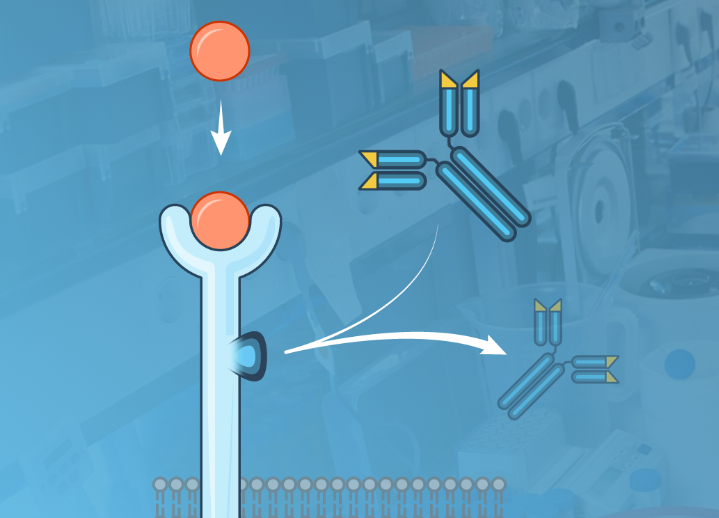
利用基因编辑工具对健康HSC细胞进行工程化,改变HSC表面的CD45的某单一氨基酸,使其成为一种CD45变体,并不影响原本的功能;但是CD45 CAR-T并不会结合该CD45变体,从而实现CD45 CAR-T能够杀死表达CD45的肿瘤细胞,而不影响正常的HSC。
这种CAR-T细胞与工程化HSC的组合被称为细胞屏蔽与配对免疫技术 ,目前Cimeio公司已经在多种靶标上(例如CD45、CD123、CD117等)上进行了相关的研究,表明通过对HSC细胞表面蛋白的工程,可以保护其免受靶向疗法(包括抗体、T细胞接合剂、ADC和CAR-T)的攻击。除了CD45 CAR-T,Cimeio公司还在开发CD45靶向抗体偶联药物,配合其配对免疫HSC技术,用于治疗血液肿瘤和自身免疫性疾病等适应症。
小编简评:尽管在这种组合疗法在概念上可以成立,临床前研究也提供了一定的数据支持;但是真正用到人体上,存在的风险因素还是很大;此外其复杂的治疗方案可能会产生更高的治疗成本和研发支出,以及监管的挑战。简而言之,临床转化具有较大的挑战。

上个月,Saar Gill博士和Carl June教授合作发表在Science Translational Medicine上的一篇文章,展示了这种CAR-T细胞与CD45表位编辑HSC的临床前数据。
利用CRISPR腺嘌呤碱基编辑技术在HCS上进行表位编辑,使其成为CD45变体,CD45表位编辑的HSC在体内具有持续和分化能力,且不会被CD45 CAR-T所识别和攻击,且CD45 CAR-T能够正常识别肿瘤细胞,包括急性髓系白血病、B细胞淋巴瘤和急性T细胞白血病细胞。然后将工程HSC与CD45 CAR-T配合回输小鼠,观察到这种方法成功杀死血液系统恶性肿瘤并重建了造血系统。
小编简评:尽管在这种组合疗法在概念上可以成立,或许在临床前研究中也可以提供一定的数据支持;但是真正用到人体上,存在的风险因素还是很大;此外其复杂的治疗方案可能会产生更高的治疗成本和研发支出,以及监管的挑战。
事实上,基于CD45的广泛表达以及生物学功能,能够通过调节淋巴细胞存活、细胞因子反应和TCR信号传导来控制免疫功能,也正在成为部分研究团队和公司所关注的治疗靶点。
总部位于马萨诸塞州的Magenta Therapeutics,正在开发CD45 ADC药物。正在进行IND申请,用于自身免疫性疾病,移植排斥反应等;Fred Hutchinson Cancer Center使用抗体(Anti-CD45 Monoclonal Antibody BC8-B10)进行非恶行疾病的临床研究;Perron等正在开发CD45抑制剂211 (2-[(4-acetylphenyl) amino]−3- chloronaphthoquinone)。
