导语
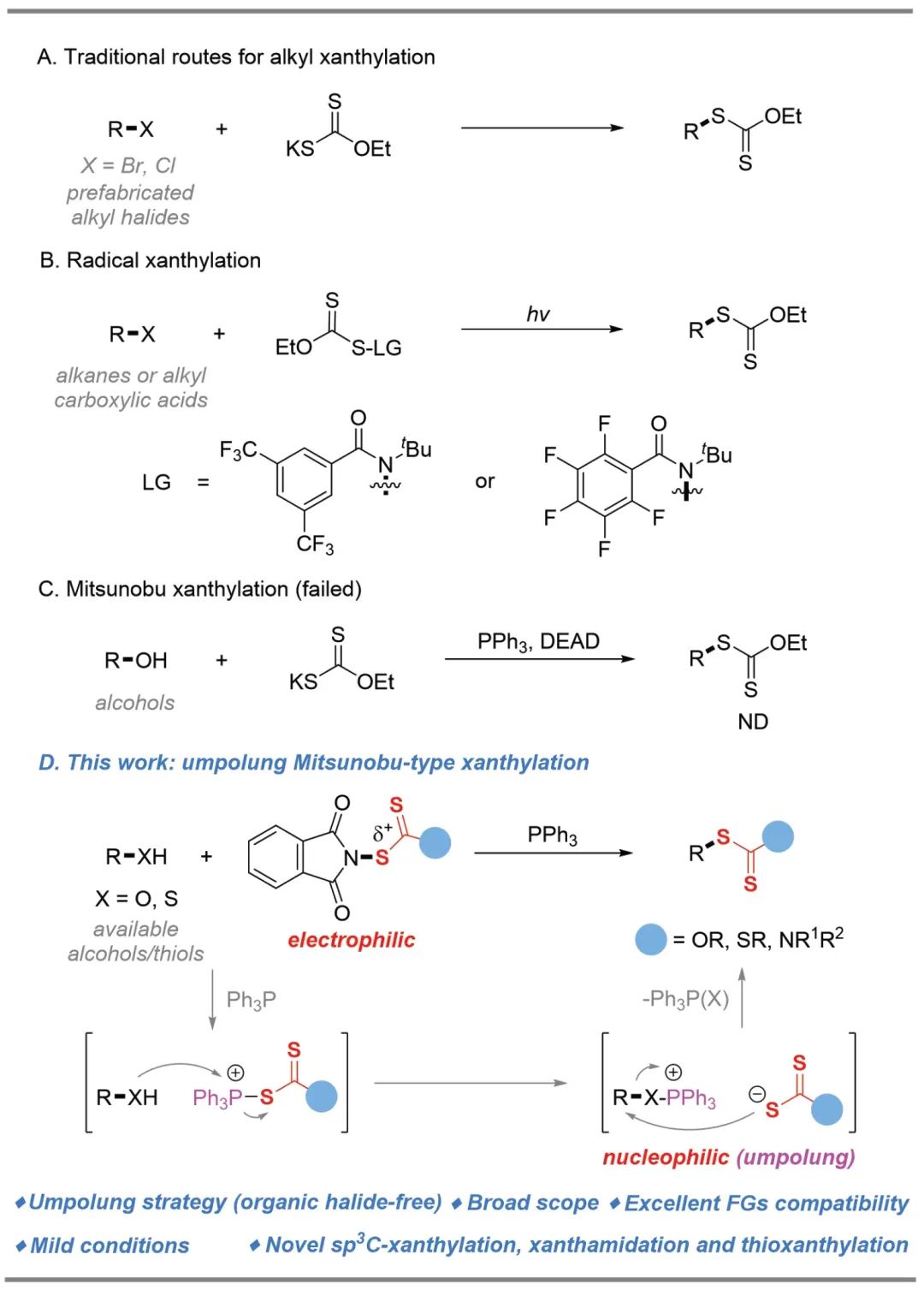
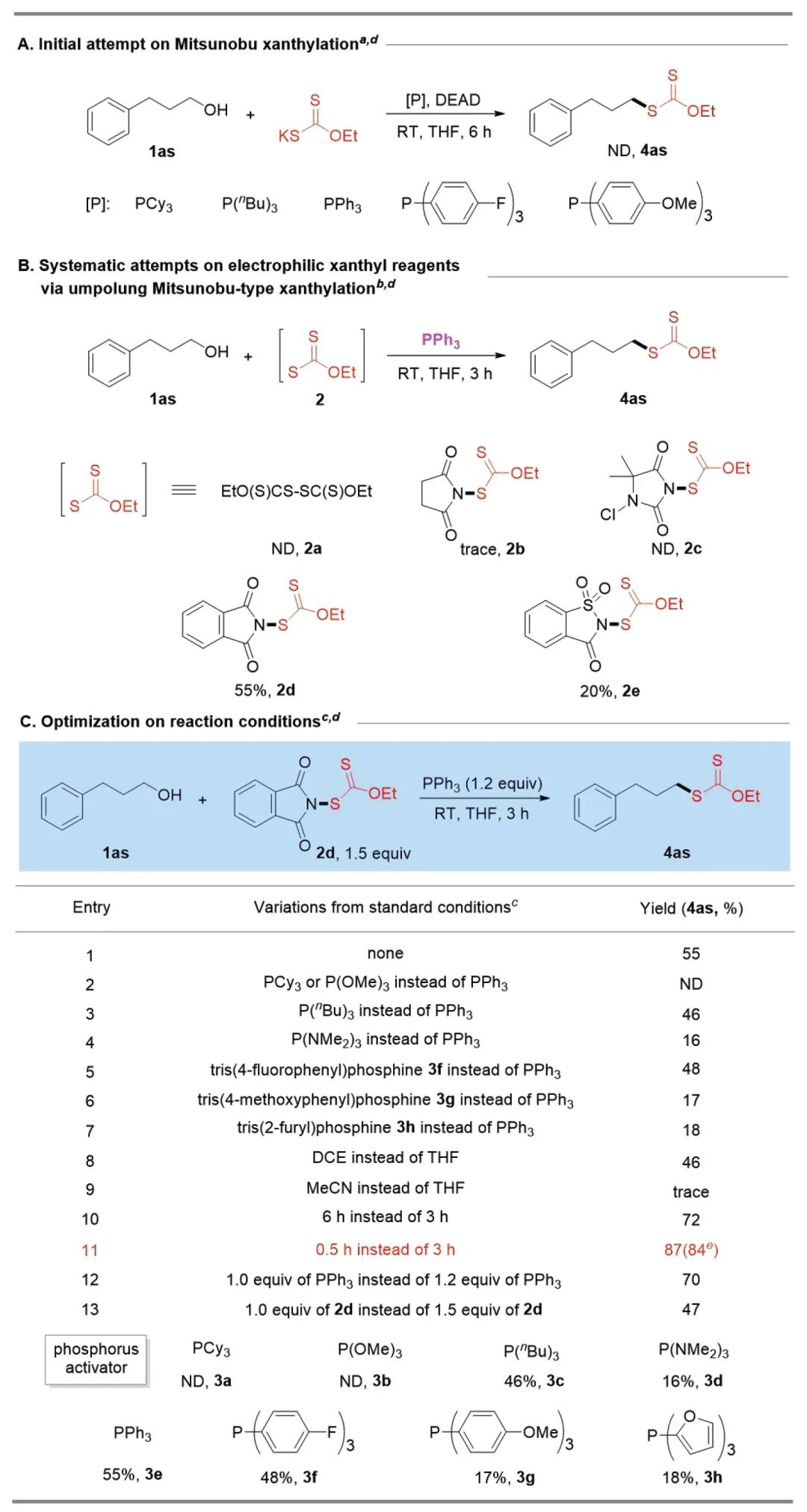
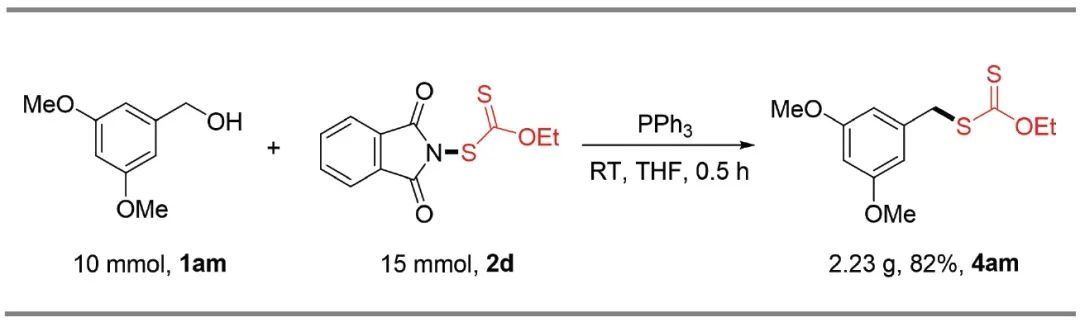
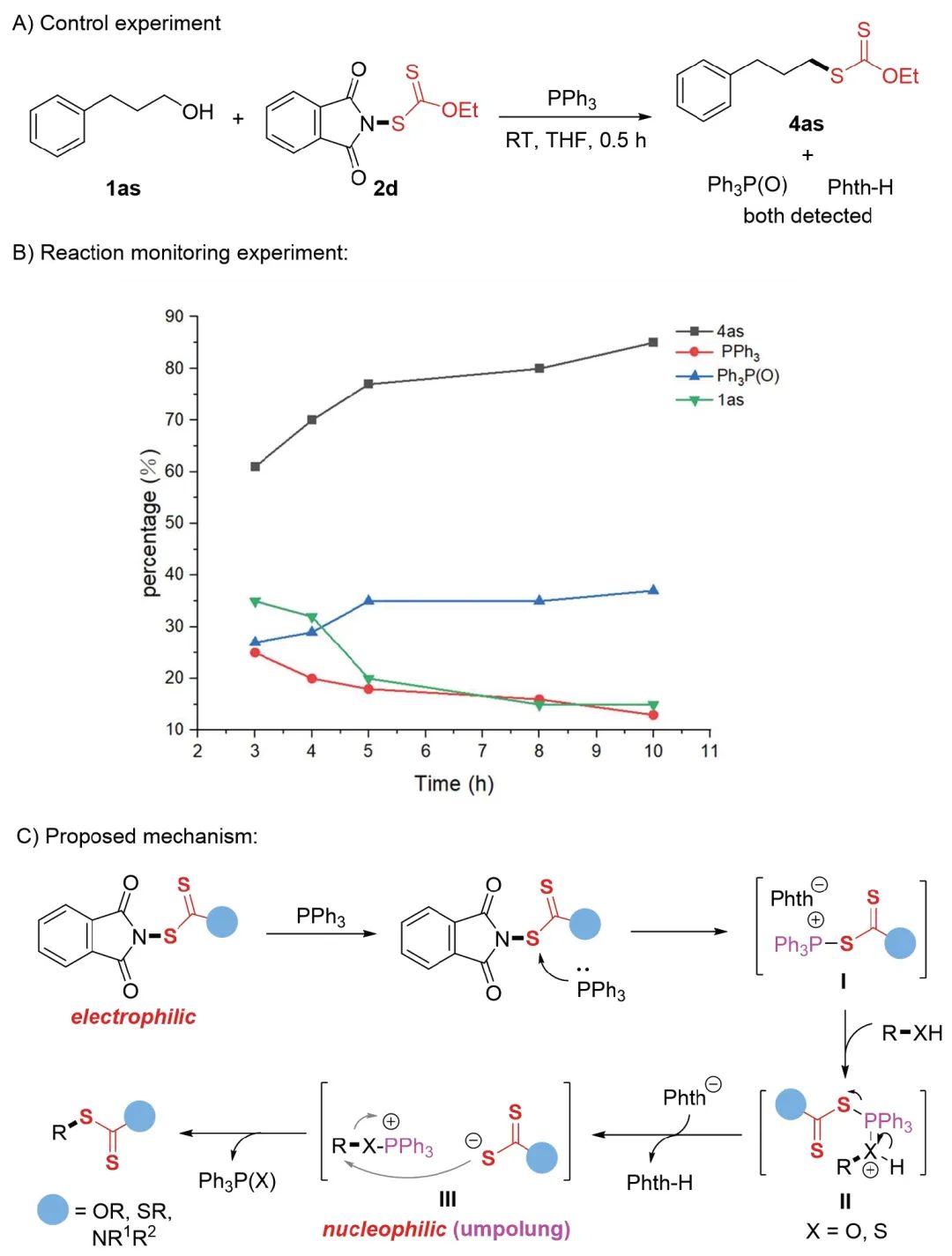
烷基黄原酸酯被广泛用作有机合成中间体,可以在合成化学中方便地转化成其他重要的官能团衍生物。利用自然界中大量易得的醇进行脱羟基黄原酸酯化反应代表了烷基黄原酸酯一种很有前途的合成方法,但很少被探索,主要是由于其挑战性的活化模式。近日,西北大学朱佃虎课题组发展了在温和条件下,利用易于获取和室温稳定的亲电性N-乙基黄原酸酯邻苯二甲酰亚胺通过极性反转的策略,实现了一级和二级醇的直接脱羟基黄原酸酯化反应,具有出色的官能团兼容性,可以兼容对还原剂敏感的氰基和硝基、未受保护的活性基团(-NH2和-OH)以及双键和三键等。和传统策略相比,这种不需使用卤化物的Mitsunobu型反应方法为有机合成中合成烷基黄原酸酯化合物提供了一条新的绿色途径。此外,脂肪族硫醇也可以成功地进行脱巯基黄原酸酯化反应来产生相应的sp3C-黄原酸酯化产物。值得注意的是,黄原酰胺和黄原酸硫酯基团也可以通过这种策略转化为所需的烷基底物。广泛的底物范围、出色的官能团相容性和生物活性分子的后期功能化使该方法作为一种新型有吸引力的策略,可以快速地将SC(S)R(R = OEt,Oalkyl,NEt2和SEt)连接在复杂的烷基链上。相关成果以“Direct Dehydroxy(sulfhydryl)xanthylation of Alcohols and Thiols”为题发表在Organic Chemistry Frontiers(2024, DOI: 10.1039/D4QO00608A)。

前沿科研成果
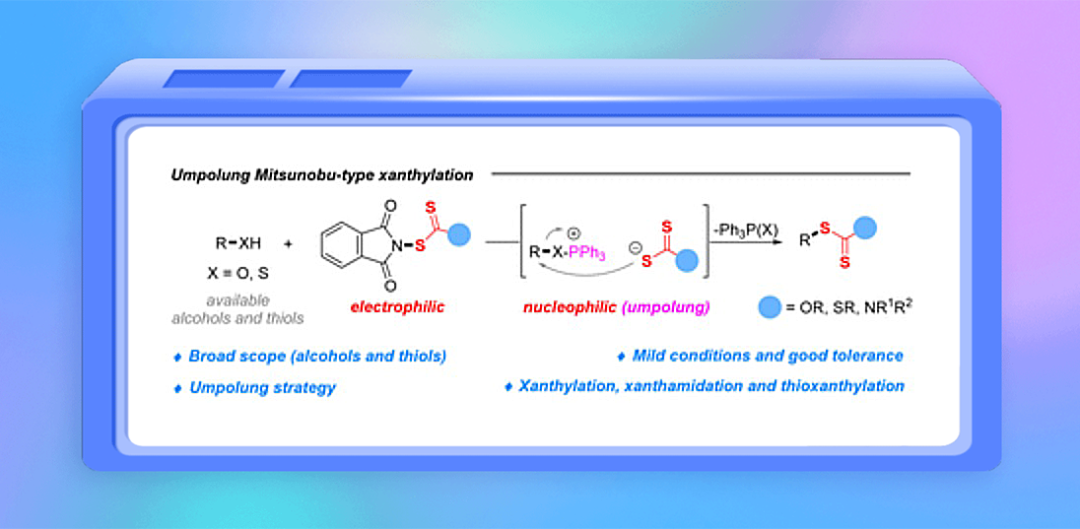
醇和硫醇的直接脱羟基(巯基)黄原酸酯化反应